Υγεία
ΕΜΑ για εμβόλιο Johnson & Johnson: Την επόμενη εβδομάδα οι αποφάσεις
Το σκεύασμα έχει ανασταλεί στις ΗΠΑ μετά την εμφάνιση περιστατικών θρομβώσεων. Καθυστερήσεις στη διανομή δόσεων στην Ευρώπη ανακοίνωσε η φαρμακευτική εταιρεία.
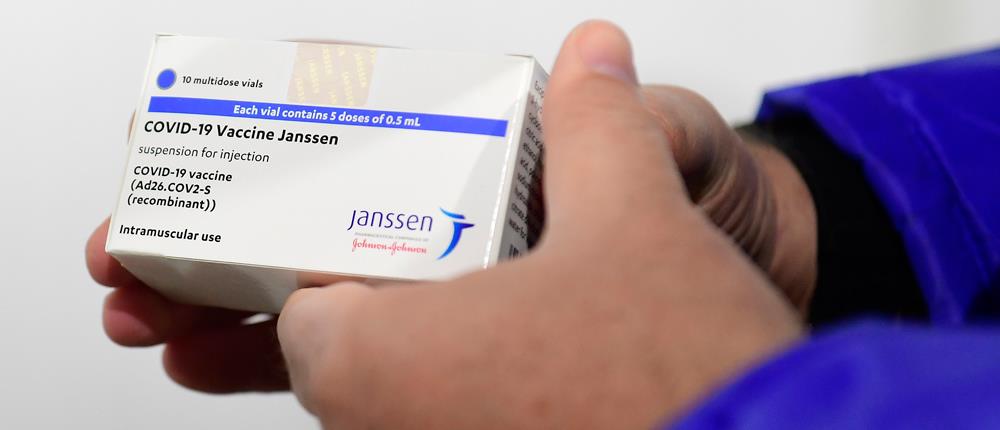
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (ΕΜΑ) προβλέπει να κάνει ανακοινώσεις την επόμενη εβδομάδα για το εμβόλιο Janssen (της εταιρείας Johnson & Johnson) για την Covid-19, η χρήση του οποίου ανεστάλη χθες στις Ηνωμένες Πολιτείες και τη Νότια Αφρική, λόγω της εμφάνισης σπάνιων, αλλά σοβαρών, θρομβοεμβολών.
«Ο ΕΜΑ ερευνά όλες τις περιπτώσεις που έχουν αναφερθεί και θα αποφασίσει εάν είναι αναγκαία κάποια ρυθμιστική ενέργεια». Επί του παρόντος «προβλέπει να δημοσιοποιήσει μια σύσταση την επόμενη εβδομάδα», ανακοίνωσε ο Οργανισμός, ο οποίος προς το παρόν θεωρεί ότι τα πλεονεκτήματα είναι περισσότερα από τους κινδύνους.
Το μονοδοσικό εμβόλιο της Johnson & Johnson έχει πάρει άδεια χρήσης στην Ευρωπαϊκή Ένωση (με την ονομασία Janssen), αλλά δεν έχει ξεκινήσει ακόμη η χορήγησή του. Η εταιρεία από την πλευρά της αποφάσισε να καθυστερήσει τη διανομή του στην Ευρώπη.
Το εμβόλιο αυτό ήταν το τέταρτο που έλαβε άδεια χρήσης στην Ευρώπη, τον περασμένο μήνα, μετά από εκείνα των Pfizer/BioNTech, Moderna και AstraZeneca/Οξφόρδης.
«Ενώ η έρευνά του είναι σε εξέλιξη, ο ΕΜΑ παραμένει της άποψης ότι τα πλεονεκτήματα του εμβολίου για την πρόληψη της Covid-19 υπερτερούν του κινδύνου εμφάνισης παρενεργειών», σημειώνεται στην ανακοίνωση.
Η ανταποκρίτρια του ΑΝΤ1 στις Βρυξέλλες, Μαρία Αρώνη, μεταδίδει:
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (ΕΜΑ) ανακοίνωσε σήμερα ότι συνεχίζει και επιταχύνει την αξιολόγηση των "πολύ σπάνιων" περιπτώσεων θρόμβων αίματος, μετά τη χορήγηση του εμβολίου Janssen κατά του covid19 και αναμένεται να εκδώσει σύσταση την επόμενη εβδομάδα. Στην ανακοίνωσή του ο ΕΜΑ υπενθυμίζει ότι την προηγούμενη εβδομάδα ανακοινώθηκε ότι η επιτροπή ασφάλειάς του (PRAC) εξετάζει πολύ σπάνιες περιπτώσεις ασυνήθιστων θρόμβων αίματος που εμφανίστηκαν μετά τη χορήγηση του εμβολίου Janssen κατά του covid19 στις ΗΠΑ. Υπενθυμίζει, επίσης, ότι ο Οργανισμός Φαρμάκων των ΗΠΑ (FDA) και το CDC συνέστησαν χθες να διακοπεί η χρήση του εμβολίου, ενώ εξετάζονται έξι αναφερόμενες περιπτώσεις στις ΗΠΑ. Έχουν χορηγηθεί πάνω από 6,8 εκατομμύρια δόσεις του εμβολίου.
Επιπλέον, ο ΕΜΑ σημειώνει ότι η εταιρεία J&J ανακοίνωσε την απόφασή της να καθυστερήσει προληπτικά τις παραδόσεις εμβολίων στην ΕΕ, καθώς συνεχίζονται οι έρευνες. Το εμβόλιο εγκρίθηκε στην ΕΕ στις 11 Μαρτίου, αλλά η ευρεία χρήση του εντός της ΕΕ δεν έχει ακόμα ξεκινήσει. Η εταιρεία βρίσκεται σε επαφή με τις εθνικές αρχές, συνιστώντας να αποθηκεύσει τις δόσεις που έχουν ήδη ληφθεί έως ότου η αρμόδια επιτροπή ασφαλείας του ΕΜΑ εκδώσει σύσταση.
Η ανακοίνωση καταλήγει ως εξής:
«Ο ΕΜΑ διερευνά όλες τις περιπτώσεις που αναφέρθηκαν και θα αποφασίσει αν απαιτείται κανονιστική δράση. Ο Οργανισμός συνεργάζεται στενά με το FDA των ΗΠΑ και άλλους διεθνείς ρυθμιστικούς φορείς. Ο ΕΜΑ επιταχύνει αυτήν την αξιολόγηση αι επί του παρόντος αναμένει να εκδώσει σύσταση την επόμενη εβδομάδα. Ενώ η αναθεώρησή του βρίσκεται σε εξέλιξη, ο ΕΜΑ παραμένει της άποψης ότι τα οφέλη του εμβολίου στην πρόληψη του covid19 υπερτερούν των κινδύνων παρενεργειών. Η επιστημονική γνώμη του Οργανισμού παρέχει στα κράτη μέλη της ΕΕ τις πληροφορίες που χρειάζονται για τη λήψη αποφάσεων σχετικά με τη χρήση εμβολίων στις εθνικές εκστρατείες εμβολιασμού τους».
Κορονοϊός: ο “χάρτης” με τα κρούσματα της Τετάρτης
Αλλαγές στα σχολεία: Αγγλικά στο νηπιαγωγείο και μάθημα για σεξουαλική αγωγή
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (ΕΜΑ) ανακοίνωσε σήμερα ότι συνεχίζει και επιταχύνει την αξιολόγηση των "πολύ σπάνιων" περιπτώσεων θρόμβων αίματος, μετά τη χορήγηση του εμβολίου Janssen κατά του covid19 και αναμένεται να εκδώσει σύσταση την επόμενη εβδομάδα.
Στην ανακοίνωσή του ο ΕΜΑ υπενθυμίζει ότι την προηγούμενη εβδομάδα ανακοινώθηκε ότι η επιτροπή ασφάλειάς του (PRAC) εξετάζει πολύ σπάνιες περιπτώσεις ασυνήθιστων θρόμβων αίματος που εμφανίστηκαν μετά τη χορήγηση του εμβολίου Janssen κατά του covid19 στις ΗΠΑ. Υπενθυμίζει, επίσης, ότι ο Οργανισμός Φαρμάκων των ΗΠΑ (FDA) και το CDC συνέστησαν χθες να διακοπεί η χρήση του εμβολίου, ενώ εξετάζονται έξι αναφερόμενες περιπτώσεις στις ΗΠΑ. Έχουν χορηγηθεί πάνω από 6,8 εκατομμύρια δόσεις του εμβολίου.
Επιπλέον, ο ΕΜΑ σημειώνει ότι η εταιρεία J&J ανακοίνωσε την απόφασή της να καθυστερήσει προληπτικά τις παραδόσεις εμβολίων στην ΕΕ, καθώς συνεχίζονται οι έρευνες. Το εμβόλιο εγκρίθηκε στην ΕΕ στις 11 Μαρτίου, αλλά η ευρεία χρήση του εντός της ΕΕ δεν έχει ακόμα ξεκινήσει. Η εταιρεία βρίσκεται σε επαφή με τις εθνικές αρχές, συνιστώντας να αποθηκεύσει τις δόσεις που έχουν ήδη ληφθεί έως ότου η αρμόδια επιτροπή ασφαλείας του ΕΜΑ εκδώσει σύσταση.
Η ανακοίνωση καταλήγει ως εξής:
«Ο ΕΜΑ διερευνά όλες τις περιπτώσεις που αναφέρθηκαν και θα αποφασίσει αν απαιτείται κανονιστική δράση. Ο Οργανισμός συνεργάζεται στενά με το FDA των ΗΠΑ και άλλους διεθνείς ρυθμιστικούς φορείς. Ο ΕΜΑ επιταχύνει αυτήν την αξιολόγηση αι επί του παρόντος αναμένει να εκδώσει σύσταση την επόμενη εβδομάδα. Ενώ η αναθεώρησή του βρίσκεται σε εξέλιξη, ο ΕΜΑ παραμένει της άποψης ότι τα οφέλη του εμβολίου στην πρόληψη του covid19 υπερτερούν των κινδύνων παρενεργειών. Η επιστημονική γνώμη του Οργανισμού παρ΄ρεχει στα κράτη μέλη της ΕΕ τις πληροφορίες που χρειάζονται για τη λήψη αποφάσεων σχετικά με τη χρήση εμβολίων στις εθνικές εκστρατείες εμβολιασμού τους».